

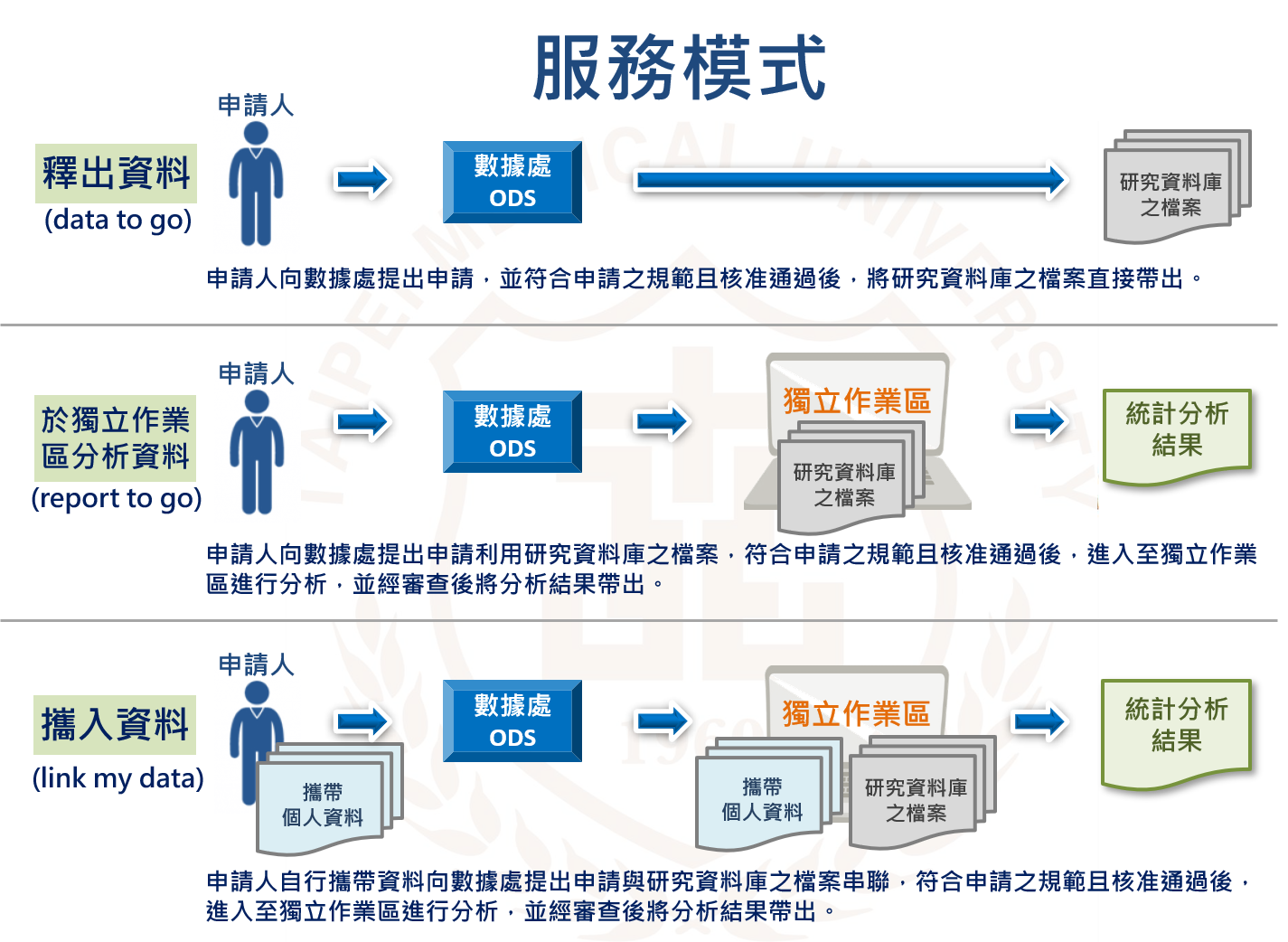
服務模式
|
提出申請所需文件 | 釋出資料條件 |
通知案件資料完成時所需文件或載具 |
備註 |
|---|---|---|---|---|
| 釋出資料(data to go) | 1. 申請單APP02及欄位勾選表 2. IRB證明函及計畫書 3. 諮詢單APP01 |
1. 申請之資料為臨床研究資料庫之資料。 2. 諮詢單載明篩選研究對象之操作型定義,須於各附屬醫院之病人數均大於五人,且各附屬醫院之病歷數均小於各院總病歷數之百分之一。 |
1. 保密切結書APP05 (申請單全部人員) 2. 釋出單APP04 |
1. 申請書研究主題需與IRB計畫名稱一致。 2. 申請者需於釋出單簽名確認內容。 3. 校務研究不適用釋出資料服務模式,請改其他服務模式辦理。 |
服務模式
|
提出申請所需文件 | 攜出報表條件 | 通知案件資料完成時所需文件或載具 | 備註 |
|---|---|---|---|---|
| 於獨立作業區分析資料(report to go) | 1. 申請單APP02及欄位勾選表 2. IRB證明函及計畫書 |
基於統計揭露控制原則,報表變項分類過細少於一單位以下、可回推出少於一單位以下或以特殊符號註記之統計分析結果均不得攜出,不得自行利用攜出之統計分析結果,產製一單位以下之統計結果。 | 1. 保密切結書APP05 (申請單全部人員) 2. 案件專用3.5吋硬碟 |
1. 如需初估樣本數先評估研究可行性,請至dBI查詢或填寫諮詢單APP01。 2. 申請書研究主題需與IRB計畫名稱一致。 3. 需親至受管制之獨立作業區分析資料,請事先預約座位。 |
服務模式
|
提出申請所需文件 | 攜出報表條件 | 通知案件資料完成時所需文件或載具 | 備註 |
|---|---|---|---|---|
| 攜入資料(linked my data) | 1. 申請單APP02及欄位勾選表 2. IRB證明函及計畫書 3. 特定對象知情同意書(Informed consent) |
基於統計揭露控制原則,報表變項分類過細少於一單位以下、可回推出少於一單位以下或以特殊符號註記之統計分析結果均不得攜出,不得自行利用攜出之統計分析結果,產製一單位以下之統計結果。 | 1. 保密切結書APP05 (申請單全部人員) 2. 案件專用3.5吋硬碟 |
1. 申請書研究主題需與IRB計畫名稱一致。 2. 審查過程將會抽查特定對象知情同意書正本,驗後立刻歸還。 3. 特定對象識別代碼(如身分證字號、病歷號碼)。 4. 攜入檔案應與IRB文件上所提之檔案名稱、資料筆數、欄位名稱及譯碼簿應一致。 5. 需親至受管制之獨立作業區分析資料,請事先預約座位。 |